Сроки рецензирования в летнее время
В связи с отпускным периодом большинства сотрудников редакции и рецензентов, срок обработки и рецензирования рукописей научных работ, поступающих в редакцию «Сибирского онкологического журнала» в июле-августе, может превышать установленный срок.

Научно-практический рецензируемый журнал
Сибирский онкологический журнал
Учредитель: Федеральное государственное бюджетное научное учреждение «Томский национальный исследовательский медицинский центр Российской академии наук»
Регистрация: в Федеральной службе по надзору в сфере связи, информационных технологий и массовых коммуникаций. Свидетельство о регистрации СМИ: ПИ № ФС77-85416 от 13 июня 2023 года.
Журнал издается с 2002 г.
ISSN 1814-4861 (Print)
ISSN 2312-3168 (Online)
Периодичность: 6 номеров в год
Языки журнала: русский и английский.
Территория распространения: Российская Федерация, зарубежные страны
Журнал входит в «Перечень рецензируемых научных изданий, в которых должны быть опубликованы основные научные результаты диссертаций на соискание ученой степени кандидата наук, на соискание ученой степени доктора наук» по следующим специальностям:
- 1.5.4. Биохимия (медицинские науки)
- 3.1.6. Онкология, лучевая терапия (медицинские науки)
- 3.1.6. Онкология, лучевая терапия (биологические науки)
- 3.1.9. Хирургия (медицинские науки)
- 3.3.3. Патологическая физиология (медицинские науки)
- 3.3.6. Фармакология, клиническая фармакология (медицинские науки)
Индексация:
- Российский индекс научного цитирования (РИНЦ)
- Russian Science Citation Index (RSCI)
- Scopus с 2017 года
Журнал относится к первой категории (К1) списка Высшей аттестационной комиссии (ВАК)
Журнал входит в международные и российские электронные библиотечные системы, в том числе в Научную электронную библиотеку (elibrary.ru), электронную библиотеку «Сyberleninka», онлайн-платформу «Directory of Open Access Journals» (DOAJ).
Распространяется на условиях Creative Commons Attribution 4.0 License: полнотекстовые материалы доступны в открытом доступе.
Краткая аннотация: научно-практический рецензируемый журнал публикует обзоры, лекции, оригинальные статьи, краткие сообщения, заметки из практики по клинической и экспериментальной онкологии.
Журнал освещает вопросы канцерогенеза, молекулярной биологии, эпидемиологии, профилактики, комбинированной диагностики, современного лечения опухолей (хирургии, химиотерапии, радиотерапии, комбинированного лечения), анестезиологического обеспечения, медицинской и социальной реабилитации, паллиативной помощи и «качества жизни» онкологических больных.
Текущий выпуск
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
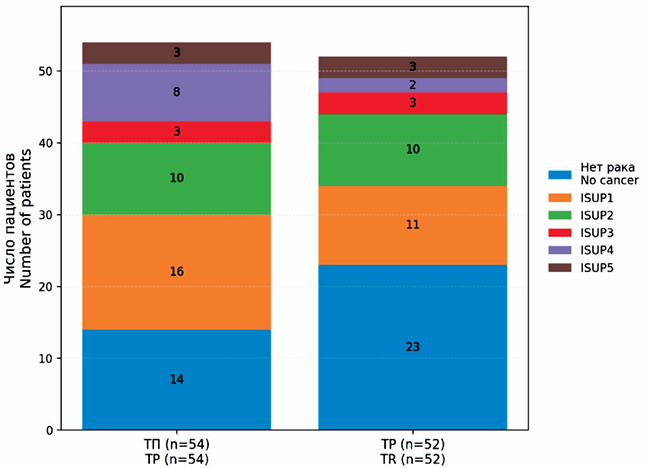
Цель исследования – сравнить диагностическую эффективность, безопасность и переносимость трансперинеальной (ТП) и трансректальной (ТР) биопсий предстательной железы, выполняемых амбулаторно под местной анестезией.
Материал и методы. В рандомизированное контролируемое исследование включено 106 мужчин с подозрением на рак простаты. Пациенты случайным образом распределены в группы ТП (n=54) и ТР (n=52). Всем выполнена систематическая 12-точечная биопсия; при наличии очагов PI-RADS ≥3 – таргетная биопсия. Антибиотикопрофилактика назначалась только в ТР-группе. Первичной конечной точкой была частота выявления клинически значимого рака (ISUP ≥2). Вторичные исходы: общая детекция рака, осложнения (Clavien–Dindo), болевой синдром (ВАШ), длительность процедуры и удовлетворенность.
Результаты. Рак обнаружен у 74,1 % пациентов группы ТП и у 55,8 % – группы ТР (p=0,066). Клинически значимый рак – у 44,4 и 34,6 % соответственно (p=0,33). Инфекционные осложнения отмечены только после ТР-биопсии (11,5 vs 0 %; p=0,012); тяжелых осложнений не зарегистрировано. Легкие осложнения (гематурия, гематоспермия) встречались одинаково часто (30 %). Боль по ВАШ была ниже при ТП (медиана 3 vs 5, p<0,01); сильная боль (ВАШ ≥6) – у 6 % ТП против 33 % ТР. Длительность процедуры составила 20 мин для ТП и 8 мин для ТР (p<0,001). Удовлетворенность пациентов была высокой в обеих группах (85 и 75 %, p=0,20).
Заключение. ТПбиопсия показала сопоставимую с ТР диагностическую эффективность при меньшем риске инфекций и более низком уровне боли. Несмотря на большую длительность процедуры, удовлетворенность пациентов оставалась высокой. Полученные данные поддерживают применение трансперинеальной биопсии как более безопасного метода в амбулаторной практике.
Цель исследования – оценка диагностических и прогностических возможностей технологии QClamp™ real-time ПЦР для выявления цоДНК с мутациями гена KRAS у пациентов с протоковой аденокарциномой поджелудочной железы.
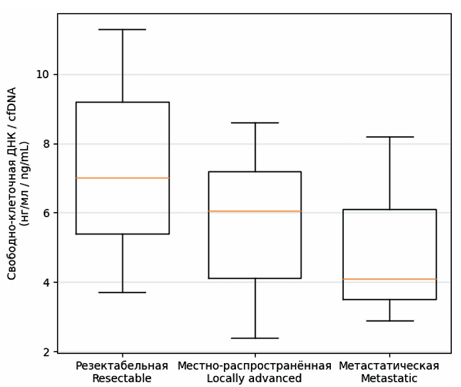
Материал и методы. В исследование включено 119 пациентов с различной распространенностью рака поджелудочной железы (РПЖ). Из плазмы крови выделяли внеклеточную ДНК и проводили детекцию наиболее распространенных соматических мутаций KRAS с использованием XNA-опосредованного подавления амплификации дикого типа.
Результаты. Мутации KRAS в плазме крови выявлены у 23,5 % пациентов, при этом частота обнаружения цоДНК возрастала с прогрессированием заболевания и достигала при местнораспространенном РПЖ – 66,7 % и при метастатическом – 25,0 %. У больных с резектабельными стадиями (I–II) рака поджелудочной железы цоДНК выявлялась в 15,6 % случаев, однако ее наличие было ассоциировано с достоверно худшей общей и безрецидивной выживаемостью. Концентрация общей внеклеточной ДНК существенно варьировала и не коррелировала напрямую со стадией заболевания, что подтверждает ограниченную информативность этого показателя без молекулярного анализа.
Заключение. Полученные данные свидетельствуют, что QClamp™ ПЦР является быстрым и технически выполнимым методом детекции цоДНК, обладающим высокой специфичностью. Наибольшее клиническое применение технология может иметь в прогнозировании течения заболевания и мониторинге минимальной остаточной болезни после хирургического лечения, дополняя существующие клинико-инструментальные подходы.
Введение. Рабдомиосаркома параменингеальной локализации с интракраниальным распространением характеризуется агрессивным течением и высоким риском лептоменингеального метастазирования (ЛМ). Исторически поражение центральной нервной системы (ЦНС) считалось инкурабельным состоянием с выживаемостью, не превышающей 10–20 %. Основным препятствием для проникновения большинства лекарственных препаратов и создания эффективной концентрации является гематоэнцефалический барьер (ГЭБ). В связи с этим поиск эффективных и нетоксичных методов контроля над лептоменингеальными метастазами является одной из наиболее актуальных задач детской онкологии. Интратекальная химиотерапия (ИТХТ), заключающаяся в прямом введении цитостатиков в спинномозговую жидкость, позволяет обойти ГЭБ и создать высокие терапевтические концентрации препаратов непосредственно в очаге поражения при минимальной системной токсичности.
Цель исследования – оценить эффективность и безопасность интратекальной химиотерапии в комплексном лечении детей с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием и улучшить показатели выживаемости данной когорты детей.
Материал и методы. В исследование был включен 21 пациент с гистологически верифицированным диагнозом рабдомиосаркомы параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием, получавший лечение в НИИ детской онкологии и гематологии им. акад. Л.А. Дурнова в период с 2021 по 2024 г.
Результаты. При медиане наблюдения 34,3 мес общая 2-летняя выживаемость составила 65 %. Данный показатель определялся высокой эффективностью раннего контроля над опухолевыми клетками за гематоэнцефалическим барьером: общая 2-летняя выживаемость достигла более 80 % как в группе профилактической, так и в группе терапевтической интратекальной химиотерапии первой линии. Это достоверно выше по сравнению с группой рецидива, где общая 2-летняя выживаемость составила 20 % (p<0,05), и существенно превосходит данные, представленные в зарубежной литературе о медиане выживаемости – 4–6 мес при лептоменингеальном метастазировании [1]. Профиль токсичности ИТХТ был благоприятным, без случаев тяжелой нейротоксичности.
Заключение. Интенсивная интратекальная химиотерапия в комплексном лечении детей с рабдомиосаркомой параменингеальной локализации с интракраниальным распространением и/или лептоменингеальным метастазированием является эффективным и безопасным методом контроля над опухолевыми клетками за гематоэнцефалическим барьером, позволяющим значительно улучшить выживаемость в этой прогностически крайне неблагоприятной группе пациентов.
ЛАБОРАТОРНЫЕ И ЭКСПЕРИМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Патогенные мутации в генах репарации ДНК (таких как BRCA1/2, RAD50, RAD51D, PTEN и др.) ответственны за развитие наследственного рака молочной железы и яичников. Большое количество вариантов, выявляемых с помощью технологии NGS, имеют неизвестное или конфликтное клиническое значение. Реклассификация данных вариантов играет решающую роль в рутинной лабораторной практике.
Целью исследования явилась реклассификация варианта конфликтного значения гена RAD51D (rs145309168), обнаруженного у молодой пациентки бурятского происхождения с раком молочной железы, с использованием нонсенс-опосредованного распада мРНК (NMD) с последующим секвенированием по Сэнгеру.
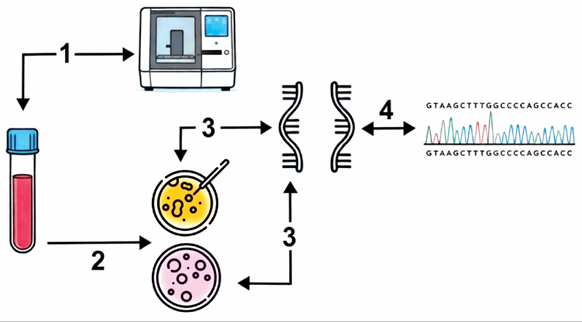
Материал и методы. Полноэкзомное секвенирование (WES) было выполнено на ДНК, выделенной из цельной крови 16 пациенток с раком молочной железы бурятского этноса, у которых отсутствовали мутации в генах BRCA1/2 (данные не представлены). Диагноз пациенток подтвержден морфологически (T1–3N0–2M0). У всех обследованных женщин был диагностирован инвазивный (протоковый) рак молочной железы неспецифического типа. Патогенные варианты, ассоциированные с заболеванием, не выявлены. Далее были проанализированы редкие варианты (MAF<0,005) для оценки их влияния на сплайсинг РНК с использованием биоинформатических инструментов, таких как SpliceAI, ESEFinder, RESCUE-ESE и EX-SKIP. Редкий миссенс-вариант в гене RAD51D (rs145309168) был идентифицирован у 39-летней пациентки бурятского этноса с раком молочной железы. Замороженные лейкоциты этой пациентки были разделены на две группы: экспериментальную и контрольную. Образцы культивировали в течение 5–6 дней и обрабатывали пуромицином (только экспериментальную группу) в течение 4–6 ч перед выделением РНК для предотвращения NMD с последующим секвенированием по Сэнгеру.
Результаты. In vitro эксперименты проводились на живых лейкоцитах пациентки с раком молочной железы, имеющей вариант c.932T>A гена RAD51D. Ампликоны кДНК были получены из РНК, выделенной из контрольных и экспериментальных лейкоцитов (обработанных пуромицином для предотвращения деградации, опосредованной NMD). Для точной оценки аберраций сплайсинга транскрипты экспериментальных лейкоцитов сравнивались с транскриптами контрольных культур лейкоцитов с помощью секвенирования по Сэнгеру. Последовательности транскриптов кДНК сравниваемых образцов в обоих случаях сохраняют изучаемый вариант, что указывает на то, что вариант не активирует NMD и, следовательно, не влияет на сплайсинг.
Заключение. В данном исследовании впервые представлен in vitro анализ варианта RAD51D (rs145309168), найденного у молодой пациентки бурятского этноса с раком молочной железы. Наши экспериментальные данные демонстрируют, что вариант c.932T>A не нарушает нормальный сплайсинг, что служит основанием для реклассификации данного «Конфликтного варианта» на «Вероятно доброкачественный», что согласуется с литературными данными и данными ранних классификаций.
Актуальность. Колоректальный рак (КРР) характеризуется высокой летальностью и развитием резистентности к терапии. Перспективным направлением является применение метаболитов микробиоты, таких как индол-3-пропионовая кислота (ИПК), обладающая иммуномодулирующей и противоопухолевой активностью.
Цель исследования – оценить противоопухолевую активность индол-3-пропионата in vivo на модели колоректального рака мыши.
Материал и методы. Эксперимент проводили на 42 мышах самках с подкожным КРР CT26 (паспортизированная клеточная линия аденокарциномы толстой кишки мыши). После достижения объема опухоли 50–60 мм3 животные были рандомизированы на 6 групп (n=7): контроль (раствор 0,9 % NaCl внутрибрюшинно и внутрижелудочно), монотерапия ИПК) (6 мг/кг, внутрижелудочно), 5-фторурацил (5-FU) (25 мг/кг, внутрибрюшинно), оксалиплатин-РОНЦ (ОХА) (10 мг/кг, внутрибрюшинно), комбинации ИПК (6 мг/кг, внутрижелудочно) + 5-FU (25 мг/кг, внутрибрюшинно) и ИПК (6 мг/кг, в/ж) + ОХА (10 мг/кг, внутрибрюшинно). Препараты вводили 3 раза в нед (Пн, Вт, Пт) в течение 3 нед. Оценка результатов проводилась через 1 нед после окончания лечения. Оценивали объем опухоли и процент торможения роста опухоли (ТРО). Статистический анализ выполняли с использованием U-критерия Манна–Уитни.
Результаты. Монотерапия ИПК не оказывала значимого эффекта (ТРО=5,0 %). Химиопрепараты в монотерапии демонстрировали умеренную активность: ТРО для 5-FU – 22,9 %, для ОХА – 19,4 %. Наибольшая эффективность достигнута в группах комбинированной терапии: ТРО для ИПК + 5-FU – 31,9 %, для ИПК + ОХА – 30,1 %. Значимое торможение роста в этих группах регистрировалось с 18-го дня (на 4 дня раньше, чем при монотерапии цитостатиками). Токсичность, оцениваемая по динамике массы тела, отсутствовала во всех группах.
Обсуждение. Полученные результаты демонстрируют, что ИПК не обладает самостоятельной цитотоксической активностью в отношении опухолевых клеток линии CT26. Однако выявлен ее потенциал в комбинации со стандартными химиотерапевтическими препаратами. Более раннее и выраженное ТРО в группах с комбинированной терапией свидетельствует о способности ИПК ускорять развитие терапевтического ответа.
Заключение. ИПК потенцирует противоопухолевую активность 5-FU и ОХА на модели КРР CT26, не увеличивая системную токсичность. Полученные данные обосновывают дальнейшее изучение механизмов синергизма ИПК с химиопрепаратами и ее эффективности при других злокачественных новообразованиях.
Кислотность микроокружения опухоли представляет собой фундаментальный признак рака, способствующий прогрессированию опухоли, инвазии, уклонению от иммунного ответа и устойчивости к лечению.
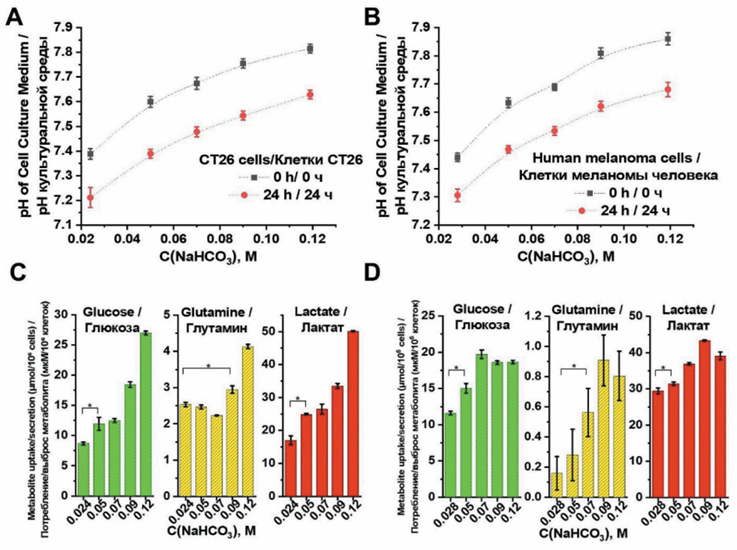
Цель исследования – изучение противоопухолевых механизмов ощелачивания гидрокарбонатом натрия на клетках аденокарциномы толстой кишки мыши CT26 и меланомы человека.
Материал и методы. Клетки подвергали воздействию различных повышенных концентраций гидрокарбоната натрия (50–119 мМ) с целью оценки его влияния на жизнеспособность, метаболизм, миграцию и пути клеточной гибели.
Результаты. Результаты показали немедленное повышение значений внеклеточного pH, зависящее от концентрации гидрокарбоната натрия, с последующим их понижением через 24 ч вследствие метаболической адаптации. Обе линии клеток демонстрировали дозозависимую цитотоксичность с концентрацией полумаксимального ингибирования примерно 80–90 мМ, при этом уровень апоптоза, определённый с помощью окрашивания Annexin V/PI, был минимален, что указывает на альтернативные механизмы клеточной гибели. Гидрокарбонат натрия значительно нарушал миграцию клеток в тестах по восстановлению монослоя и вызывал деполяризацию митохондрий, подтверждённую снижением флуоресценции зонда Mito Red. Метаболический анализ выявил повышенное потребление глюкозы и глутамина на фоне увеличенного образования лактата, что свидетельствует о метаболическом перепрограммировании в ответ на стресс ощелачивания. Несмотря на увеличение накопления лизосом, определенное с помощью зонда Lyso Green, классические маркеры аутофагии (LC3B и p62) не показали значимых изменений, свидетельствуя о том, что традиционные пути аутофагии не играют ведущей роли.
Заключение. Полученные данные указывают на то, что ощелачивание гидрокарбонатом натрия индуцирует гибель опухолевых клеток посредством механизмов, выходящих за рамки классического апоптоза и аутофагии, возможно включая лизосом-зависимую смерть или алкалиптоз. Исследование дает механистическое обоснование потенциала гидрокарбоната натрия в качестве потенциальной адъювантной терапии, направленной на кислотность микроокружения опухоли, с перспективой повышения эффективности традиционных методов лечения рака через модуляцию pH. Для полного понимания задействованных путей клеточной гибели необходимы дальнейшие исследования.
Актуальность. Раковые стволовые клетки (РСК) являются одной из причин прогрессирования и рецидивов колоректального рака (КРР). Детальное изучение фенотипа данных клеток, их иммунобиологических свойств необходимо для разработки методов лечения КРР.
Цель исследования – определить содержание РСК, имеющих фенотип EpCAMhighCD44+, в первичной опухоли у больных КРР, а также экспрессию на их поверхности CD133, CD166, CD24 и CD184.
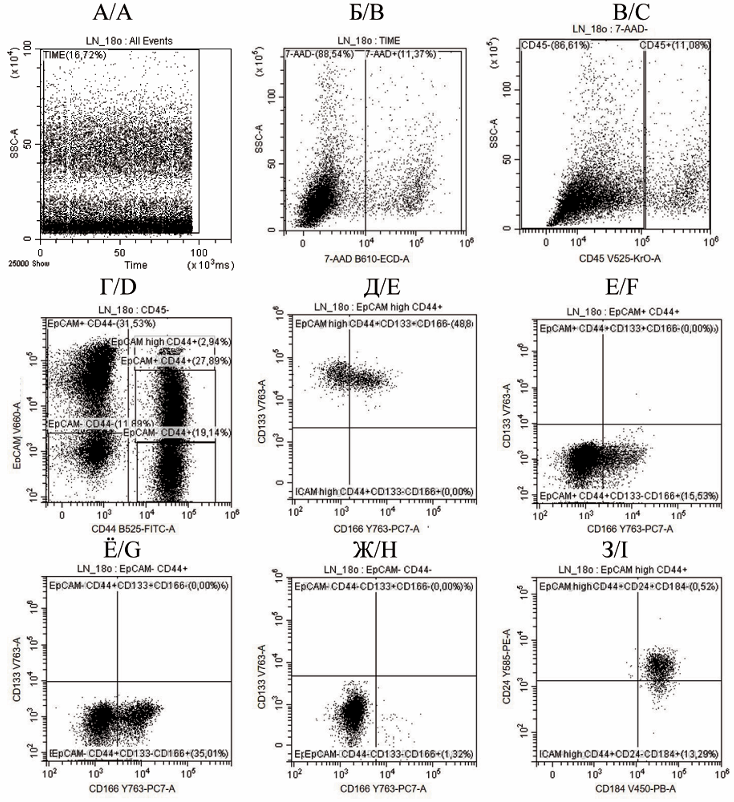
Материал и методы. Выполнено одномоментное поперечное исследование клеточного состава опухолевой ткани 123 больных аденокарциномой толстой кишки III cтадии. Контрольную группу составили 87 больных, оперированных по поводу неопухолевых заболеваний толстой кишки. Для получения суспензии клеток опухолевой ткани использовали ферментативный метод. Гейтирование клеток нелимфоидного происхождения (CD45- ) производили в зависимости от экспрессии на их поверхности молекулы адгезии эпителиальных клеток EpCAM и дифференцировочного антигена CD44. Экспрессия EpCAM, CD44, СD133, CD166, СD184 и CD24 на РСК исследована методом проточной цитометрии.
Результаты. Относительное содержание РСК с фенотипом CD45- EpCAMhighCD44+ в опухолевой ткани при КРР составило 17,15 [11,76; 26,44] % от пула клеток нелимфоидного происхождения. У больных КРР в структуре РСК обнаружено 42,83 [37,07; 51,77] % клеток, одновременно экспрессирующих СD133 и CD166, и 57,17 [48,23; 62,93] % клеток, экспрессирующих дифференцировочный антиген CD133. Все РСК в первичной опухоли экспрессируют CD184, и 95,18 [88,48; 97,98] % из них одновременно экспрессируют CD24. При высокодифференцированной аденокарциноме количество клеток EpCAMhighCD44+ в первичной опухоли в 1,5 раза ниже по отношению к умеренно дифференцированному КРР (U=326,5, p=0,002) и в 2,1 раза (U=21,0, p<0,001) – по сравнению с низкодифференцированной аденокарциномой. У пациентов c КРР IIIС стадии на 13 % увеличивается количество опухолевых клеток с фенотипом EpCAMhighCD44+CD133+CD166+ по отношению к больным КРР IIIВ стадии (U=1116,0, p=0,007).
Заключение. В первичной опухоли при КРР раковые стволовые клетки, высокоэкспрессирующие молекулу адгезии эпителиальных клеток EpCAM и CD44, составляют 17,2 % от пула клеток нелимфоидного происхождения. Количество опухолевых клеток EpCAMhighCD44+ увеличивается при снижении степени дифференцировки аденокарциномы.
Введение. Экспрессия основных медиаторов воспалительного сигналинга – цитокинов и длинных некодирующих РНК (днРНК) – играет значительную роль в течении опухолевого процесса и формировании платинорезистентного фенотипа рака яичников (РЯ).
Цель исследования – оценить коэкспрессию длинных некодирующих РНК HOTAIR, MALAT1, PVT1 с провоспалительными цитокинами в плазме крови как признак возможного формирования платинорезистентного фенотипа рака яичников.
Материал и методы. В исследование включено 46 пациенток с первичным раком яичников, проходивших лечение в Ульяновском онкологическом диспансере в 2018–21 гг., и 12 пациенток с доброкачественными опухолями яичников (группа сравнения). Из 2 мл плазмы крови пациенток до начала лечения выделяли РНК с последующими обратной транскрипцией и полимеразной цепной реакцией для анализа экспрессии HOTAIR, MALAT1, PVT1. В плазме крови также определяли уровни цитокинов IL-1β, -10, -17A, -18. Пациентки c РЯ были разделены на 2 группы по продолжительности бесплатинового интервала.
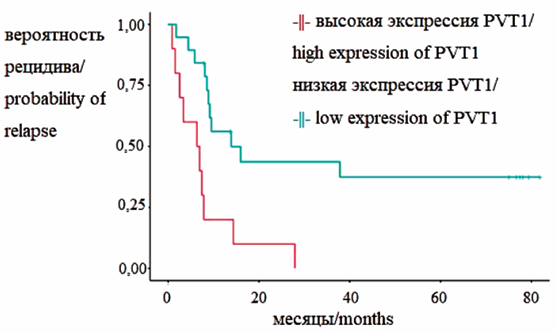
Результаты. Установлено, что экспрессия в плазме длинных некодирующих РНК HOTAIR, MALAT1, PVT1 у больных раком яичников значимо выше, чем в плазме у пациенток с доброкачественными опухолями яичников. Экспрессия HOTAIR в плазме крови также была выше при раке яичников III–IV стадии, чем при РЯ I–II стадии. У пациенток с платинорезистентным раком яичников был значимо ниже уровень IL-17A и IL-10 по сравнению с группой сравнения, но выше IL-1β и IL-10, чем у больных платиночувствительным РЯ. Установлена корреляция между экспрессией днРНК MALAT1 и уровнем цитокина IL-18 в сыворотке крови.
Заключение. Уровень экспрессии днРНК PVT1 в сыворотке крови пациенток с РЯ коррелирует со временем выживания без прогрессирования и позволяет оценить вероятность рецидива заболевания. Сочетанный уровень коэкспрессии днРНК MALAT1 и IL-18 в сыворотке крови может быть использован как предиктивный маркер для выявления платинорезистентного РЯ, а их сочетанная гиперэкспрессия с провоспалительными цитокинами до начала химиотерапии обладает прогностическим потенциалом маркера платинорезистентности рака яичников. В модель оценки риска прогрессирования РЯ в первые 6 мес от постановки диагноза включены данные экспрессии MALAT1 и HOTAIR и сывороточные уровни IL-1β, -18 до начала терапии, при этом значение коэффициента (К) выше 1,65 свидетельствует о высоком риске прогрессирования заболевания.
ОПЫТ РАБОТЫ ОНКОЛОГИЧЕСКИХ УЧРЕЖДЕНИЙ
Актуальность. Лучевая терапия является одним из основных методов лечения злокачественных новообразований, эффективность которого зависит от соотношения доз излучения, поглощенных опухолевыми и здоровыми клетками. Качество дозиметрического плана традиционно оценивается на основе физико-дозиметрических критериев, однако для достижения максимального прогнозируемого терапевтического эффекта необходимо учитывать радиобиологические аспекты. Существующее разнообразие радиобиологических моделей и отсутствие единого подхода к систематизации их численных параметров затрудняют их практическое применение, что делает актуальной задачу создания специализированной базы данных.
Цель исследования – разработка базы данных клинически значимых радиобиологических показателей опухолей и нормальных тканей для фотонной и нейтронной терапии как единого специализированного инструмента для повышения точности дозиметрического планирования и прогнозирования клинических результатов лечения злокачественных новообразований.
Материал и методы. Проведен анализ более 100 научных работ из открытых источников, посвященных расчетам клинически значимых радиобиологических показателей широко используемых радиобиологических моделей. В ходе исследования данные систематизированы с учетом различных режимов фракционирования, энергии и вида излучения, методик лучевой терапии, локализации и объема области облучения, а также индивидуальных особенностей пациентов.
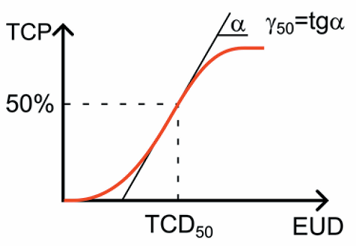
Результаты. Создана база данных клинически значимых радиобиологических показателей для фотонной и нейтронной терапии. На основе структурированных данных разработано веб-приложение с использованием языков программирования Python и JavaScript. Веб-приложение интегрировано в программное обеспечение «Калькулятор TCP/NTCP» и обеспечивает возможность хранения, быстрого поиска и анализа радиобиологических показателей.
Заключение. Созданная база данных систематизирует клинически значимые радиобиологические показатели и предоставляет специалистам единый инструмент для прогнозирования вероятного результата лечения и оценки риска нежелательных последствий для критических органов и тканей. Данный инструмент может применяться в клинической практике, образовательных программах для подготовки специалистов в области медицинской физики и лучевой терапии, а также для углубленного изучения радиобиологических эффектов и разработки новых методов лечения.
ОБЗОРЫ
Цель исследования – провести систематический анализ современных данных об эпидемиологии и факторах риска рака молочной железы (РМЖ), разработать стратегию профилактики для групп высокого риска, составить клинический профиль молодых пациенток с РМЖ и описать особенности их лечения и реабилитации.
Материал и методы. Поиск проводился в базах данных Web of Science, PubMed, Scopus, Google Scholar. В обзоре использовано 60 источников (систематические обзоры, метаанализы, рандомизированные клинические исследования), оцениваемое вмешательство представляло сравнительный анализ факторов риска, клинической картины, диагностики, лечения и реабилитации РМЖ у молодых пациенток и пациенток старшего возраста.
Результаты. Рак молочной железы является серьезной проблемой для женщин в возрасте до 40 лет, являясь второй по значимости причиной смертности от рака в этой возрастной группе во всем мире. При этом наблюдается тревожная тенденция к увеличению заболеваемости РМЖ у молодых женщин. Отсутствие программ скрининга, ориентированных на молодых женщин, приводит к диагностике РМЖ на более поздних стадиях, что негативно сказывается на клинических исходах и увеличивает риск осложнений лечения по сравнению с пациентками старшего возраста. Патоморфология опухолей, выявленных у молодых женщин, характеризуется низкой дифференцировкой клеток, повышенной экспрессией Ki67, наличием генных мутаций и преобладанием HER2-позитивных и трижды негативных иммуногистохимических подтипов. Несмотря на очевидные различия, исследований РМЖ у молодых женщин недостаточно, что создает пробелы в понимании его факторов риска, диагностики, прогноза и лечения. Отсутствие репрезентативных клинических данных с возрастной стратификацией и доказательной базы делает невозможным экстраполяцию стандартных протоколов лечения, валидированных для пациенток старшего возраста, на популяцию молодых женщин.
Заключение. Необходимы дальнейшие исследования для сбора возрастных клинических данных и разработки новых методов лечения рака молочной железы у молодых женщин, что позволит улучшить результаты лечения и определить перспективные направления исследований в этой области.
Цель исследования – систематизировать и представить современные данные, касающиеся использования в сравнении с другими серологическими маркерами белка эпидидимиса человека 4 (НЕ4) в качестве опухолеассоциированного маркера для уточняющей диагностики рака легкого (РЛ), прогноза эффективности лечения и мониторинга данной категории пациентов.
Материал и методы. Выполнен поиск и анализ доступных отечественных и англоязычных источников по базам данных РИНЦ и PubMed по ключевым словам «lung cancer (рак легкого)» и «HE4». В обзор включено 70 работ, опубликованных в период с 2006 по 2024 г.
Результаты. НЕ4 принимает участие в канцерогенезе и прогрессировании ряда гинекологических опухолей, однако его роль в развитии РЛ остается малоизученной, несмотря на его выраженную экспрессию в опухолевой ткани. Современные исследования демонстрируют, что НЕ4 по своим диагностическим характеристикам сравним или несколько превосходит другие маркеры, применяемые в диагностике РЛ (CYFRA21-1, РЭА, NSE, ProGRP и др.). В ряде работ отмечено, что сывороточный уровень НЕ4 может служить предиктором ответа на химиотерапию, продолжительности безрецидивного интервала при РЛ. Отдельные исследования свидетельствуют о целесообразности применения НЕ4 как маркера мониторинга больных РЛ для раннего выявления рецидива. Вместе с тем, показатели диагностической и прогностической значимости НЕ4 значительно варьируют в разных работах, что обусловлено разнородностью включенных групп обследуемых, различиями в используемых референсных значениях и методах оценки уровней этого маркера. Это не позволяет принять единый диагностический алгоритм использования НЕ4.
Заключение. Накопленные к настоящему времени данные свидетельствуют о возможности и целесообразности применения НЕ4 в качестве опухолеассоциированного маркера при РЛ. Однако целый ряд аспектов, важных для практического применения НЕ4 как опухолевого маркера, остаются неясными. Таким образом, внедрение этого маркера в клиническую практику требует проведения дальнейших систематизированных и углубленных исследований.
Введение. За последнее десятилетие представления о биологии HER2-негативного рака молочной железы существенно изменились благодаря выделению категорий HER2-low и HER2-ultralow, которые приобрели клиническое значение после появления антитело-лекарственных конъюгатов нового поколения.
Цель исследования – систематизировать современные сведения о молекулярных и морфологических особенностях этой группы опухолей, обсудить диагностические сложности, связанные с интерпретацией низких уровней экспрессии HER2, а также привести данные ключевых клинических исследований, определивших роль ADC в лечении пациенток с HER2-low и HER2-ultralow раком молочной железы.
Материал и методы. Поиск литературы осуществлялся в поисковых системах Medline, cochrane Library, Elibrary, включались публикации с 2004 по 2025 г.
Заключение. В настоящее время HER2-low и HER2-ultralow рак молочной железы является сложной группой опухолей. Существует ряд нерешенных вопросов, требующих детального изучения в данной области, а также формируются перспективы дальнейших исследований, направленных на совершенствование диагностики и персонализацию терапевтических подходов.
Цель исследования – проанализировать современную литературу о подходах к оценке биохимических маркеров метаболизма скелетных мышц, определить перспективные направления исследований в данной области, обозначить возможные терапевтические стратегии.
Материал и методы. Поиск литературы для подготовки обзора осуществлен по базам данных Web of Science, Scopus, Medline, the Cochrane library, РИНЦ, Pubmed. В ходе поиска проанализировано 146 источников, из них в обзор включено 47 публикаций за период 2010–2025 гг.
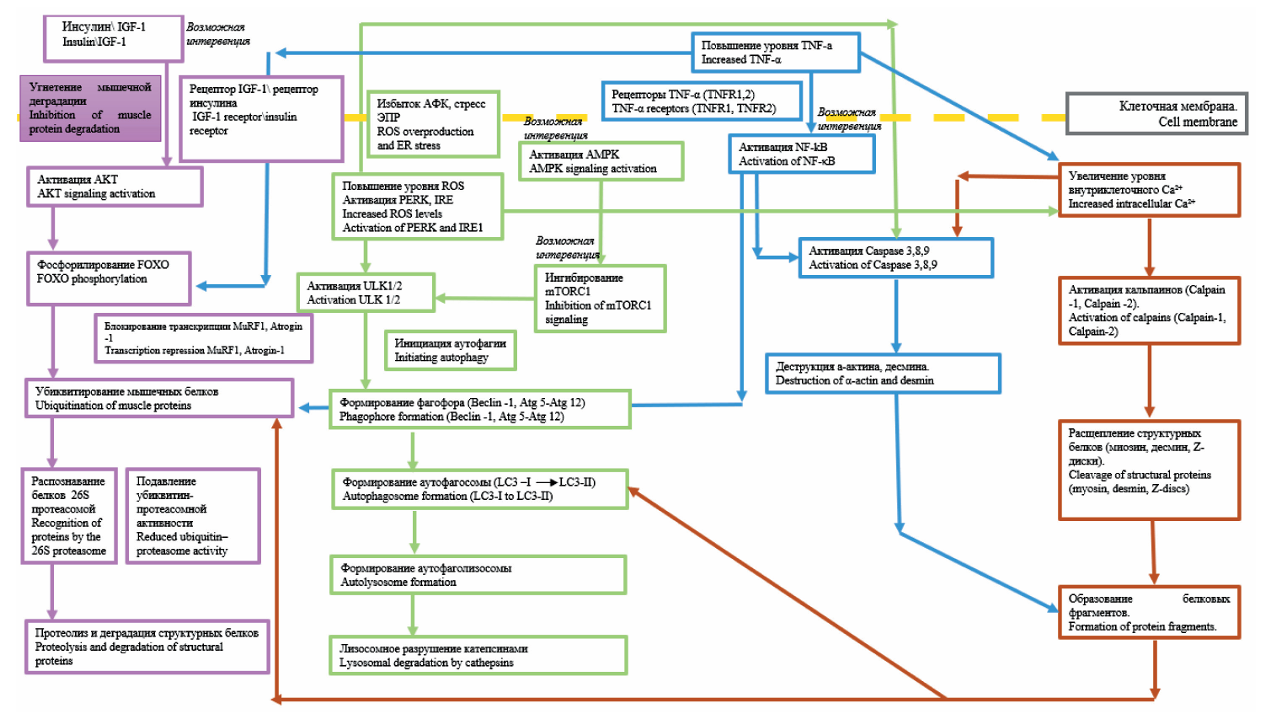
Результаты. Анализ научной литературы позволил выделить 4 ключевых протеолитических каскада, участвующих в развитии саркопении у онкологических пациентов: убиквитин-протеасомный, аутофагический, кальпаин-зависимый и каспазозависимый. Особое внимание уделено прогностической роли биохимических маркеров, включая экспрессию MuRF1 и Atrogin-1, уровни цитокинов и цистатина С. Обнаружена высокая прогностическая значимость соотношения креатинин/цистатин С в оценке риска токсичности противоопухолевой терапии и смертности. Выявлены перспективные молекулярные мишени для таргетной терапии: AMPK, сигнальные каскады IGF-1/AKT/mTOR и транскрипционный фактор NF-kB.
Заключение. Саркопения при онкологических заболеваниях обусловлена сложными и взаимосвязанными молекулярными механизмами, включающими как деградацию белка, так и нарушение регенерации мышечной ткани. Использование биохимических маркеров и таргетных вмешательств открывает перспективы для персонализированной диагностики и терапии. Необходимы дальнейшие клинические исследования для валидации биомаркеров и оценки эффективности новых терапевтических стратегий, направленных на предотвращение мышечной атрофии у онкологических больных.
Актуальность. Рак предстательной железы – одно из самых распространенных онкологических заболеваний у мужчин во всем мире. Заболевание характеризуется сложной биологией и широким спектром клинических симптомов. Последние достижения в области биоинформатики оказали значительное влияние на исследования рака, позволив интегрировать различные дисциплины и улучшить анализ биологических данных.
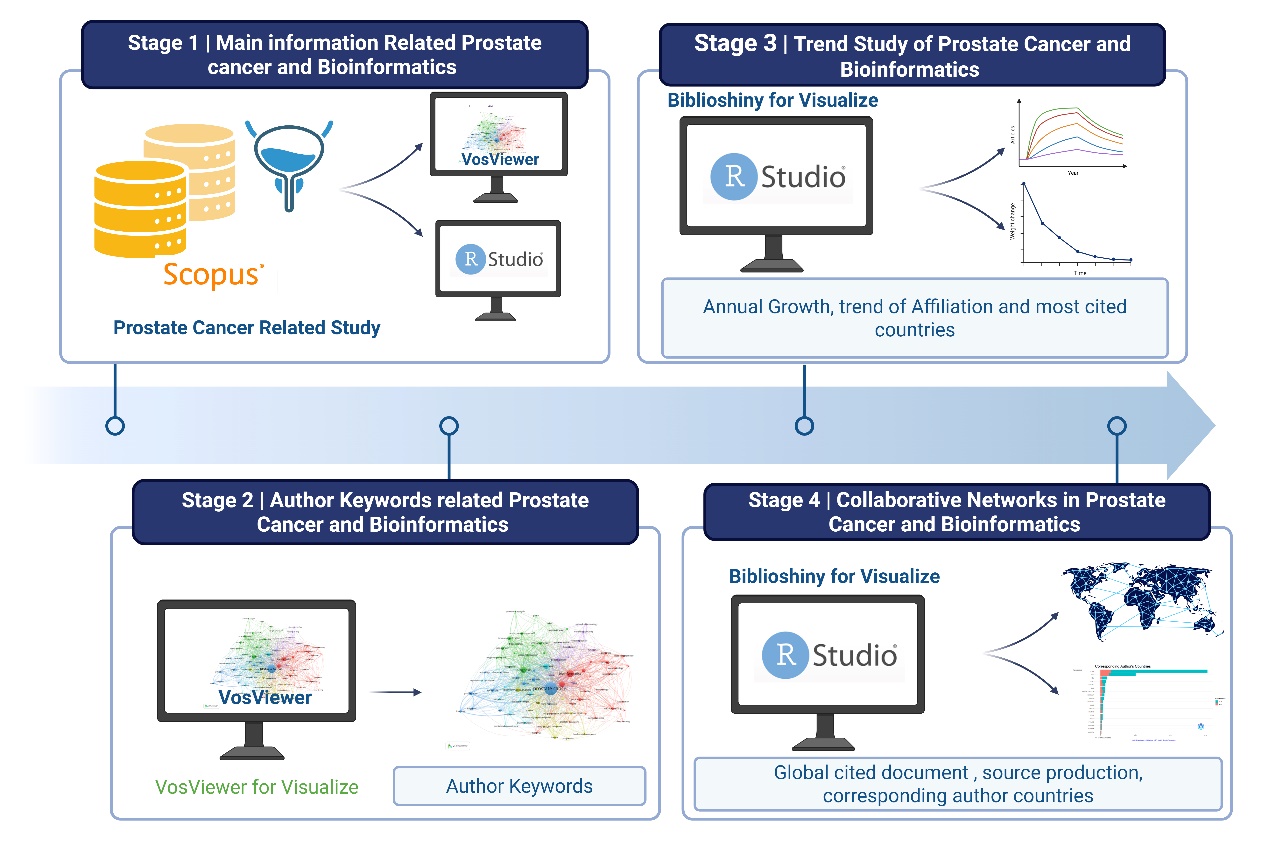
Цель исследования – представить библиометрический анализ, обобщающий глобальные тенденции исследований в области рака предстательной железы и биоинформатики с 1998 по 2025 г.
Материал и методы. Проведено библиометрическое исследование с анализом 3 426 статей, полученных из 961 издания. Проанализированы данные о результатах исследований, моделях сотрудничества, влиянии цитирования и тематических кластерах.
Результаты. Ежегодный высокий темп прироста (18,42 %), средний возраст публикации (5,65 года) и высокий показатель цитируемости (26,34) свидетельствуют о значимом влиянии на научное сообщество. Широко распространены совместные исследования: 13 598 авторов (в среднем 7,21 соавтора на публикацию). Более 21 % исследований проводится в рамках международных партнерств. Форматы публикаций включали журнальные статьи, обзоры и доклады на конференциях. Анализ ключевых слов выявил пять основных тематических кластеров: вычислительные и омиксные методологии; биология опухолей и иммунология; молекулярные механизмы и прогрессирование рака; биомаркеры и регуляция генов; междисциплинарные исследования рака. Анализ публикационной активности показал стабильный объем публикаций до 2013 г., за которым последовал заметный всплеск, достигший пика (около 500 статей) в 2023 г., чему способствовали достижения в области геномики, анализа больших данных и прецизионной онкологии. Анализ цитируемости показал, что ведущие страны по этому признаку – это США и Китай, при этом Китай лидирует по количеству публикаций, в основном за счет собственных исследований, в то время как США демонстрирует более широкое международное сотрудничество. Среди других значимых участников – Австралия, Германия, Канада, а также ряд европейских и азиатских стран.
Заключение. Исследования на стыке проблем рака предстательной железы и биоинформатики быстро развиваются, отличаются высокой степенью сотрудничества и распространены по всему миру. Многопрофильный и интегративный характер этих исследований продолжает способствовать углублению понимания, диагностики и лечения рака предстательной железы с помощью передовых биоинформатических подходов.
СЛУЧАЙ ИЗ КЛИНИЧЕСКОЙ ПРАКТИКИ
Актуальность. Люминальный рак молочной железы встречается в 60–80 % случаев и характеризуется высокой частотой метастазирования в кости, что определяет необходимость своевременного выявления отдаленных очагов. Традиционные методы визуализации имеют ограниченную чувствительность, особенно в отношении очагов малого размера. В связи с этим актуальна разработка высокочувствительных методов более ранней диагностики метастазов в кости. Перспективным направлением является таргетная радионуклидная визуализация рецептора гастрин-высвобождающего пептида (GRPR), гиперэкспрессия которого ассоциирована с рецептором эстрогена, с использованием радиофармацевтического лекарственного препарата (РФЛП) на основе антагонистов GRPR. Доклинические исследования продемонстрировали перспективность использования для этих целей РФЛП [99mTc]Tc-DB8.
Цель исследования – демонстрация возможностей РФЛП [99mTc]Tc-DB8 в диагностике костных метастазов у больных люминальным РМЖ.
Описание клинических случаев.
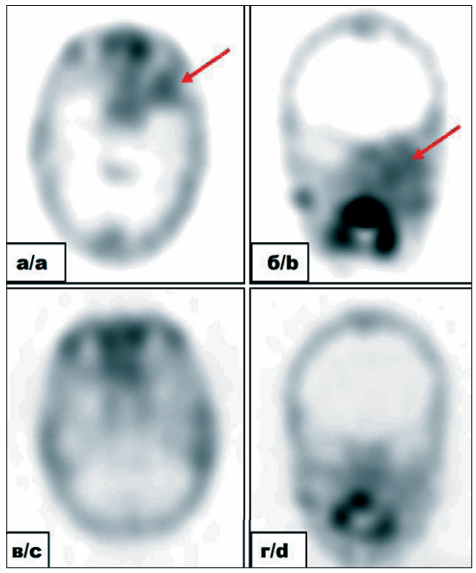
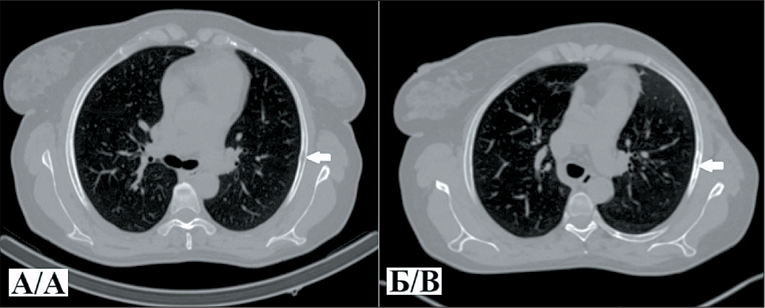
Клинический случай № 1. Пациентка К., 51 год, диагноз: Рак правой молочной железы, IIIC стадия (T2N3M0), мультицентричный рост, метастатическое поражение аксиллярных и подключичных лимфоузлов. ОФЭКТ/КТ выполнена через 2 ч после внутривенного введения РФЛП [99mTc]Tc-DB8 в дозировке протеина 80 мкг. По результатам исследования помимо первичной опухоли и метастатических лимфоузлов выявлен высокий уровень аккумуляции препарата [99mTc]Tc-DB8 в проекции V ребра справа по средней аксиллярной линии. Повторный анализ компьютерных томограмм органов грудной клетки (КТ ОГК) подтвердил наличие очага литической деструкции, расцененного как возможный метастаз и взятого под наблюдение. При КТ ОГК в динамике в указанной проекции визуализировался участок неравномерных склеротических изменений, что интерпретировано как ответ на терапию.
Клинический случай № 2. Пациентка Д., 42 года, диагноз: Рак правой молочной железы IV стадии (T1N1M1), метастаз в аксиллярный лимфоузел, множественные метастазы в костях. ОФЭКТ/КТ проведена через 2 ч после инъекции РФЛП [99mTc]Tc-DB8 в дозировке 80 мкг, при которой помимо визуализации первичного очага и метастатически измененного лимфоузла выявлена высокая аккумуляция РФЛП в проекции LII-SII, в подвздошной и седалищной костях, в заднем отрезке VII ребра справа.
Заключение. Результаты клинического исследования с использованием препарата [99mTc]Tc-DB8 продемонстрировали высокую диагностическую эффективность метода в визуализации костных метастазов у больных люминальным РМЖ.
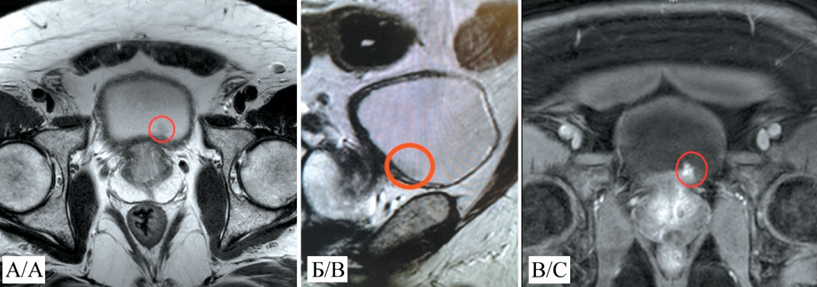
Актуальность. Агрессивная ангиомиксома (АА) – редкое мезенхимальное новообразование, преимущественно поражающее область таза и промежности у женщин репродуктивного возраста.
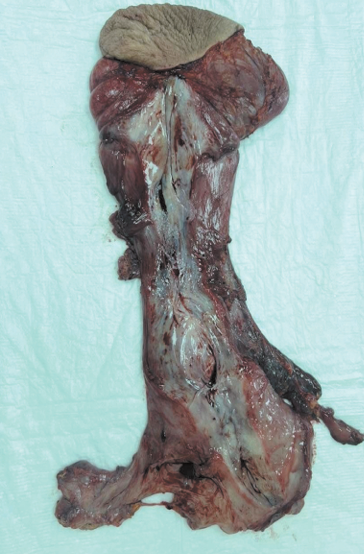
Описание клинического случая. Представлен клинический случай пациентки, 41 год, с гигантской агрессивной ангиомиксомой левой большой половой губы, размерами 300×160×60 мм. Первоначально дифференциальный диагноз проводился с кистой бартолиновой железы и паховой грыжей, однако комплексное обследование, включающее УЗИ, КТ и МРТ с контрастированием, выявило неоднородное образование с инфильтративным ростом в забрюшинное пространство. МРТ-картина демонстрировала характерные «слоистые» изменения, а гистологическое исследование подтвердило диагноз: диффузный рост опухолевых клеток в миксоматозной строме с экспрессией CD34, HMGA2 и рецепторов эстрогена/ прогестерона. Лечение включало двухэтапную операцию: наружную мобилизацию опухоли с последующей лапароскопической резекцией забрюшинного компонента новообразования и пластикой дефекта тазового дна. Гистологический анализ краев резекции и лимфатических узлов подтвердил отсутствие опухолевых клеток.
Заключение. МРТ – «золотой стандарт» диагностики АА, позволяющий оценить связь опухоли с тазовым дном. В лечении АА остаются нерешенными дилеммы, такие как радикальность резекции опухоли, частота рецидивов при которой достигает 40–50 %, что обосновывает преимущество органосохраняющих подходов. Особое внимание уделяется гормональной терапии агонистами ГнРГ и ингибиторами ароматазы – направлению, перспективному как в отношении предоперационного уменьшения объема опухоли, так и профилактики последующих рецидивов. Однако данный подход ограничен временным эффектом и побочными эффектами, что подчеркивает необходимость дальнейших исследований для стандартизации лечения и уточнения прогностической роли маркеров экспрессии HMGA2 для оценки риска рецидивов.
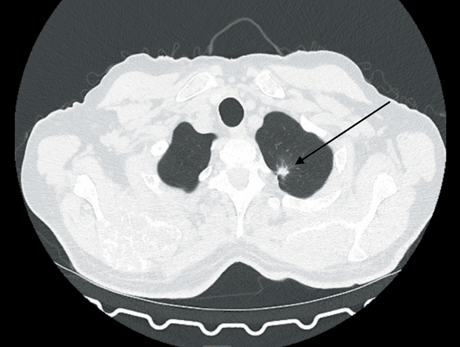
Актуальность. Согласно национальным и международным данным, рак легкого входит в число наиболее распространенных злокачественных новообразований. Значительная часть первично диагностированных случаев заболевания сопровождается наличием отдаленных метастазов.
Цель исследования – демонстрация успешного клинического случая с длительной общей и безрецидивной выживаемостью у пациента с метастатическим немелкоклеточным раком легкого (НМРЛ) при лечении комбинацией атезолизумаба с бевацизумабом и химиотерапией.
Описание клинического случая. У пациента, 72 лет, с диагнозом: Периферический немелкоклеточный (аденокарцинома) рак верхней доли правого легкого T1bN0M1b (oth), IV ст. на фоне лечения комбинацией атезолизумаба с бевацизумабом и химиотерапией получена длительная стабилизация заболевания. Общая выживаемость и выживаемость без прогрессирования составили 38 мес при достаточно благоприятном профиле безопасности.
Заключение. Даже при наличии широкого спектра современных терапевтических опций лечение метастатического НМРЛ сопряжено с определенными трудностями. Представленный клинический случай подтверждает целесообразность использования схемы, включающей атезолизумаб, бевацизумаб и химиотерапию при метастатическом НМРЛ с отрицательным статусом EGFR/ALK и отсутствием экспрессии лиганда запрограммированной клеточной гибели PD-L1.
Введение. Рак мочевого пузыря (РМП) – распространенная патология, занимает 10-е место среди всех диагностируемых онкологических образований и 1-е среди опухолей мочевыводящих путей. До 80 % случаев приходится на немышечно-инвазивный рак мочевого пузыря. Локализация опухоли мочевого пузыря (МП) по передней стенке в ряде случаев является труднодоступной для полноценной резекции стенки МП с подлежащим мышечным слоем. В качестве примера, иллюстрирующего лечение немышечно-инвазивного РМП труднодоступной локализации, представлен клинический случай пациента, находившегося на стационарном лечении в ЧУЗ ЦКБ «РЖД-Медицина» в 2022 г.
Клиническое наблюдение. В урологическом стационаре ЧУЗ ЦКБ «РЖД-Медицина» Nd:YAG-лазерная абляция немышечно-инвазивного рака мочевого пузыря труднодоступной локализации проведена пациенту, 67 лет, с образованием по передней стенке МП. При гистологическом исследовании биоптата образования мочевого пузыря верифицирован рак мочевого пузыря. Поверхностный характер роста опухоли подтвержден по результатам магнитно-резонансной томографии, проведенной до операции. Для лечения применяли Nd:YAG-лазер с длиной волны 1 064 нм, мощностью 40 Вт и плотностью энергии 100 Дж/см2 . Лазерное излучение подавалось через световод с боковым выходом (Side Fire). После операции в МП установлен двухходовый катетер на 12 ч. Интра- и послеоперационных осложнений не было. Эндоскопический мониторинг эффективности хирургического этапа лечения проводился на базе ЧУЗ ЦКБ «РЖД-Медицина» с кратностью 3, 6 и 12 мес с момента операции, при этом признаков рецидива не обнаружено.
Заключение. Анализ клинического случая позволяет сделать обоснованный вывод о достаточно высокой эффективности Nd:YAG-лазерной абляции у пациентов с немышечно-инвазивным раком мочевого пузыря с локализацией по передней стенке, что позволяет судить о безопасности использования лазерной энергии в лечении данной онкоурологической патологии.
Объявления
2024-08-12
Сроки рецензирования в летнее время
В связи с отпускным периодом большинства сотрудников редакции и рецензентов, срок обработки и рецензирования рукописей научных работ, поступающих в редакцию «Сибирского онкологического журнала» в июле-августе, может превышать установленный срок.
| Еще объявления... |
ISSN 2312-3168 (Online)